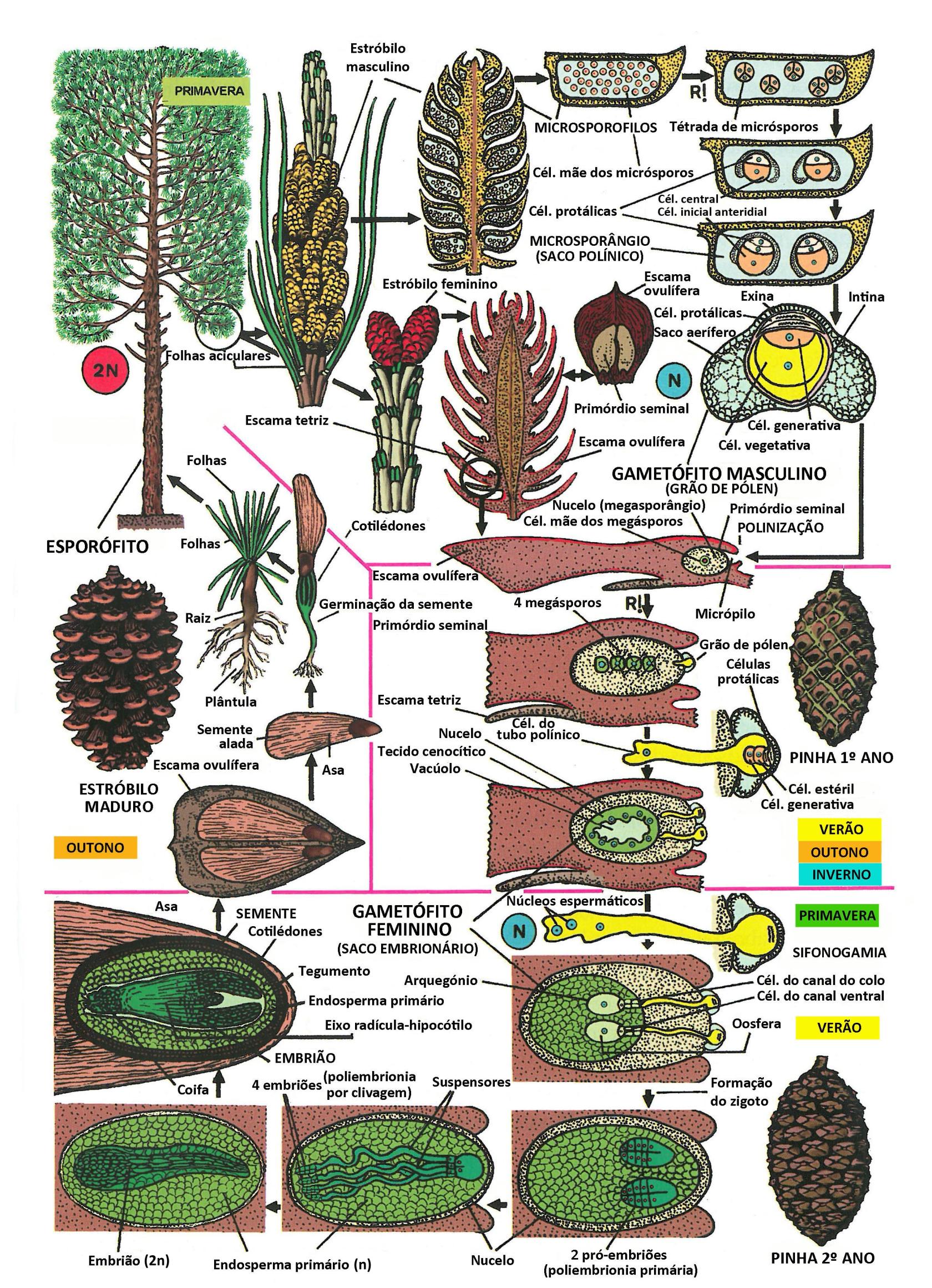
2. Ciclo de vida das gimnospérmicas
Gimnospérmicas atuais
As gimnospérmicas atuais (acrogimnospérmicas) dividem-se em cinco grandes grupos (subclasses): Cycadidae, Ginkgoidae, Cupressidae, Pinidae e Gnetidae (Figura 322). Correntemente, são aceites cerca de 1045 espécies de gimnospérmicas, repartidas por 84 géneros e 12 famílias (Christenhusz et al., 2011; Roskov et al., 2019). As 'coníferas' (Pinidae + Cupressidae) incluem a maior parte dos géneros (70) e das espécies (615). Os restantes três grupos de 'não coníferas' compreendem: 317 espécies de cicadófitos (em 10 géneros repartidos por 3 famílias); um único ginkgófito vivo (Ginkgo biloba, Ginkgoaceae); e 112 gnetófitos em três famílias monogenéricas (Ephedraceae, Welwitschiaceae e Gnetaceae).
Órgãos de suporte, estruturas reprodutivas e estróbilos
Nas gimnospérmicas, os fenómenos anatómicos e fisiológicos relacionados com a reprodução sexuada decorrem em estruturas reprodutivas unissexuais. Em contraste, as angiospérmicas possuem um órgão especializado na reprodução sexual que é originalmente hermafrodita: a flor. Nas gimnospérmicas monoicas (a condição mais frequente), cada indivíduo possui, em diferentes pontos da sua copa, estruturas reprodutivas ♂ e ♀; e.g., os pinheiros (Pinus, Pinaceae) e os abetos (Abies, Pinaceae). Nas espécies dióicas, numa mesma população coexistem indivíduos exclusivamente ♂ e indivíduos ♀; e.g., o ginkgo e o teixo (Taxus baccata, Taxaceae) (Figura 335-A).
Embora, por causa dos Pinus, a monoicia seja a condição mais comum na natureza em termos de biomassa, a maioria das espécies de gimnospérmicas é, na verdade, dioica. De modo a reduzir os riscos de autopolinização, nas espécies monoicas as estruturas reprodutivas ♀estão geralmente inseridas nos ramos localizados por cima (e a cotas mais altas) das estruturas ♂ (Niu et al., 2016).
Nas gimnospérmicas atuais, os órgãos de suporte (de sacos polínicos ou primórdios seminais) surgem, salvo raras exceções, agregados. As estruturas reprodutivas unissexuais resultantes desta agregação arquitetónica designam-se genericamente por estróbilo (ou cone) (Figuras 323 e 324). Existem duas exceções: não são, geralmente, considerados estróbilos as estruturas reprodutivas ♀ das Taxaceae nem as do ginkgo (Figuras 335-A e 326).
Como será detalhado no volume II, nas plantas com semente o saco embrionário (gametófito ♀) resulta da germinação de um megásporo confinado pelas próprias paredes do esporo (endomegasporia). Por seu turno, o gametófito ♀ germinado fica retido de forma permanente (endoprotalia) no interior do megasporângio (nucelo). Adicionalmente, este primórdio é externamente envolvido por um ou dois tegumentos de origem caulinar. Esta acumulação de camadas de proteção sobre os primórdios seminais é uma forte tendência evolutiva partilhada pelas plantas e pelos animais (Grant, 1950).
Nas angiospérmicas ocorre ainda uma camada extrema de proteção do gametófito e do gâmeta ♀: o carpelo. A solução encontrada na linhagem das gimnospérmicas teve de ser distinta, uma vez que o seu primórdio seminal (mais concretamente, o micrópilo) tem de estar fisicamente exposto ao exterior durante a polinização para captar o pólen. Assim, em grupos avançados como as araucariáceas, as 'coníferas' e as zamiáceas, o primórdio seminal está inserido (e parcialmente fundido) numa escama ou numa bráctea protetora, no âmbito de um estróbilo lenhoso. Esse mesmo estróbilo, logo após a polinização é aproveitado para proteger os primórdios fecundados e, mais tarde, já maduro, auxilia a dispersão da semente.
O termo latino strobilus refere-se originalmente a estruturas reprodutivas em forma de cone, constituídas por um eixo caulinar central, no qual se inserem escamas ou brácteas que, na maturidade, se tornam lenhosas. Com este sentido estrito, o termo é aplicado tanto às gimnospérmicas como a alguns fetos (e.g., Equisetum). Contudo, na bibliografia botânica atual, constata-se a tendência de aplicar o termo estróbilo num sentido lato a todas as estruturas reprodutivas que aglomeram órgãos de suporte de microsporângios e/ou de primórdios seminais. Sob este prisma conceptual, também a flor das angiospérmicas pode ser definida evolutivamente como um estróbilo altamente modificado e, regra geral, bissexual.
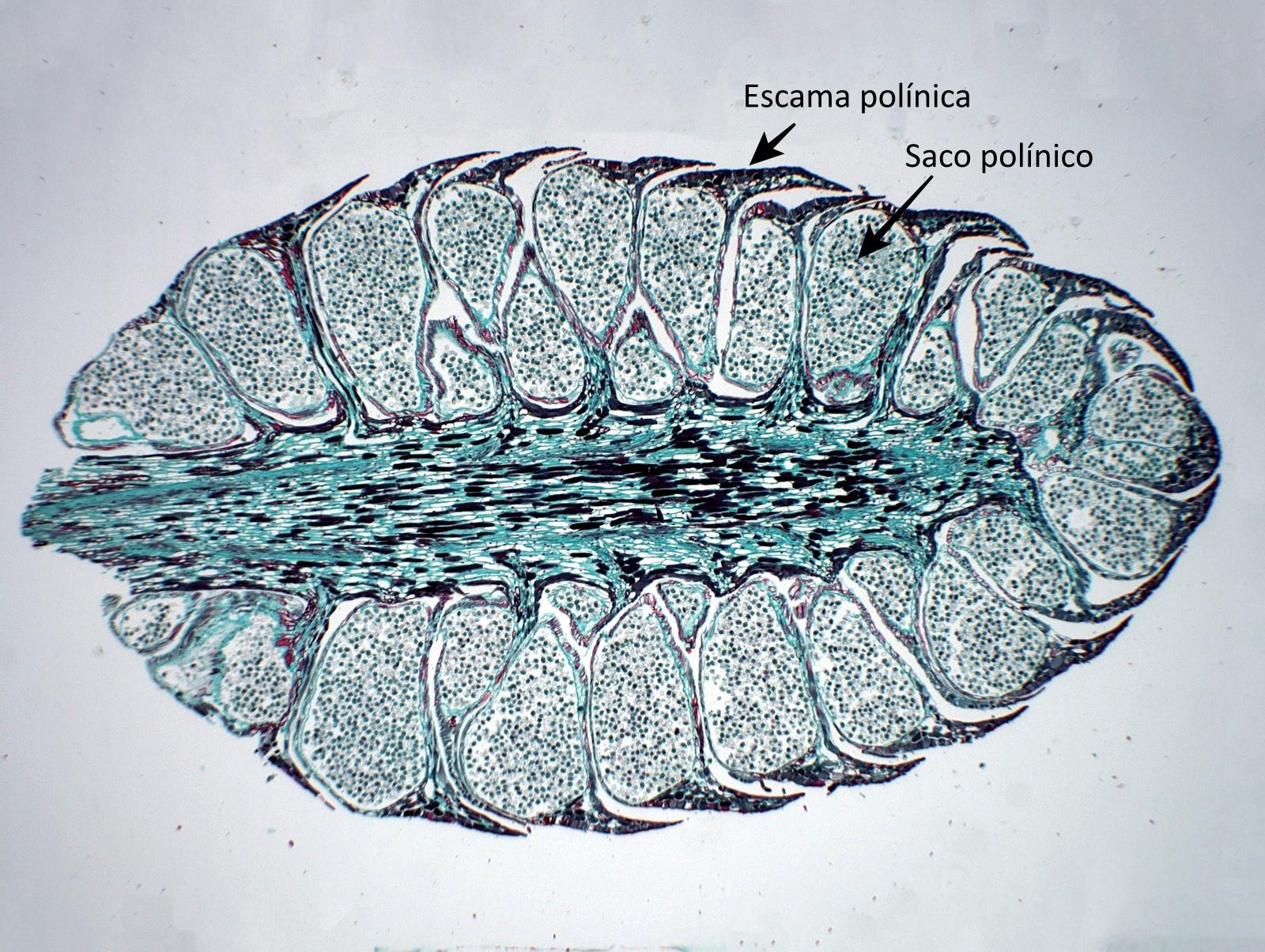
Nas plantas com semente, o pólen forma-se e matura no interior de sacos polínicos. Nas gimnospérmicas, estes sacos polínicos dispõem-se em grupos de 2 a 12 na face abaxial (inferior) de microsporofilos foliares muito especializados —as escamas polínicas (Figuras 323 e 329-A). Estes órgãos de suporte estão, por sua vez, e em número variável, sempre organizados em estróbilos ♂. Os estróbilos ♂ da esmagadora maioria das acrogimnospérmicas são anatomicamente simples (com eixos não ramificados) (Schulz et al., 2014).
Os primórdios seminais das gimnospérmicas atuais contactam diretamente o exterior — não estão encerrados num pistilo, como ocorre nas angiospérmicas. Consoante o grupo taxonómico, os primórdios seminais das gimnospérmicas apresentam-se espacialmente arrumados de quatro formas:
- Solitários, envolvidos banalmente por uma estrutura carnuda de origem foliar
,(arilo), como nas Taxaceae (com algumas exceções) (Figura 335-A); - Aos pares (raramente solitários ou em grupos de três), na extremidade de um curto ramo fértil bifurcado, como no Ginkgo (Figura 326);
- Na margem de megasporofilos pouco modificados, aglomerados em estróbilos ♀ frouxos/laxos, como no género Cycas (Cycadaceae) (Figuras 325-A e B);
- Em estróbilos ♀ compactos/congestos, geralmente lenhosos e de estrutura anatómica muito variável (vd. «Interpretação evolutiva do estróbilo ♀»; Figuras 325-C, D, 327-B, D e 329-C, D).
Na maior parte das espécies atuais — excetuando o género Cycas, o Ginkgo e a maioria das Taxaceae —, logo após a polinização, os primórdios fecundados são rapidamente envolvidos pelo crescimento de estruturas adjacentes provenientes do estróbilo ♀, as quais os isolam do exterior e os protegem de agentes bióticos e abióticos durante o longo desenvolvimento do embrião (Figura 327).
A disseminação das gimnospérmicas faz-se sob a forma de semente isolada ou sob a forma de estróbilo inteiro com assementes inclusas (vd. «Frutificações e sementes»). No primeiro caso, o estróbilo já maduro e lenhoso tem de abrir mecanicamente as suas escamas ao exterior para libertar as sementes contidas no seu interior.
Figura 323. Estrutura do estróbilo ♂ das Pinaceae. Cone ♂ de Pinus sp. (Pinaceae). N.b.: sacos polínicos preenchidos com grãos de pólen inseridos na face abaxial de escamas polínicas. [Cortesia da Cornell University Plant Anatomy Collection].
Figura 324. Estrutura do estróbilo ♀ das Pinaceae. Cone de Pinus wallichiana (Pinaceae). N.b.: no canto inferior esquerdo, escamas ovulíferas com um primórdio seminal apenso na base, axiladas por uma escama tetriz. [Cortesia da Cornell University Plant Anatomy Collection].
Interpretação evolutiva do estróbilo feminino
A interpretação evolutiva do estróbilo ♀ nos cinco grandes grupos de acrogimnospérmicas é complexa e controversa. Embora não se tenha ainda atingido uma interpretação de absoluto consenso, é hoje claro que os estróbilos, e as suas respetivas componentes anatómicas, nem sempre são estruturas homólogas entre os diferentes grupos.
Nas Cycadaceae (Cycadidae), a família de acrogimnospérmicas que retém mais características ancestrais (plesiomorfias), os primórdios seminais estão localizados na margem de megasporofilos que mantêm ainda uma nítida morfologia foliar. Estes megasporofilos, por sua vez, agrupam-se no topo dos caules, diferenciando um estróbilo ♀ laxo (Figura 325-A, B). Os primórdios seminais estão totalmente a descoberto antes da polinização, uma exposição que, nas plantas atuais, só tem equivalente no ginkgo. Nas Zamiaceae, a família mais avançada da subclasse Cycadidae, os megasporofilos estão metamorfoseados em escamas lenhosas organizadas em estróbilos muito semelhantes aos cones de algumas pináceas, com os primórdios seminais bem resguardados no seu interior (Figura 325-C). Os estróbilos ♀ dos cicadófitos dizem-se simples porque se circunscrevem a um único eixo com folhas modificadas (megasporofilos) apensas — não são caules ramificados.
O ginkgo segue um modelo anatómico completamente distinto: as estruturas reprodutivas ♀ resumem-se a um ramo fértil bifurcado (ou trifurcado), ostentando apenas 2 ou 3 primórdios seminais na extremidade distal (sendo este número maior em algumas espécies fósseis de ginkgófitos). Supõe-se que este ramo fértil seja o resultado evolutivo da hiper-simplificação de um estróbilo ♀ ancestral.
No eixo central do estróbilo ♀ das pináceas (a única família do clado dos pinófitos) inserem-se dois tipos de componentes: a bráctea tetriz (ou escama tetriz) e a escama ovulífera (Figuras 324 e 335-B, C). Cada bráctea tetriz axila (suporta na sua axila) uma escama ovulífera; por sua vez, na face adaxial (superior) de cada escama ovulífera repousam 2 primórdios seminais (Figura 335-B). O botânico sueco C. R. Florin (1894-1965) propôs que a bráctea tetriz tem origem foliar — é uma verdadeira bráctea —, sendo a escama ovulífera um sistema caulinar modificado (Florin, 1951). Odesenho e a dimensão relativa da bráctea e da escama são atributos morfológicos muito valorizados na taxonomia e segregação dos géneros de pináceas (Figura 335-C). Portanto, o estróbilo ♀ das pináceas é, na realidade, um sistema de caules, i.e., um estróbilo composto muito simplificado, desprovido de megasporofilos foliares (Figura 328-A).
Os cupressófitos são morfologicamente muito mais diversos do que os pinófitos. Comportam cinco famílias atuais: Araucariaceae, Podocarpaceae, Sciadopityaceae, Cupressaceae (que agora inclui as antigas Taxodiaceae) e Taxaceae. Na família das cupressáceas (a mais diversa do grupo), as escamas ovulíferas estão reduzidas a uma mera protuberância (invisível nas frutificações maduras) nos géneros mais basais da família (em parte das antigas taxodiáceas, e.g., Sequoia e Cryptomeria). Este resquício evolutivo caulinar desaparece por completo nos grupos mais avançados da família (as Cupressaceae s.str.). Em ambos os casos, os estróbilos ♀ das cupressáceas são constituídos por um eixo principal (por vezes muito curto) revestido por brácteas que são homólogas das brácteas tetrizes dos pinófitos — sendo, portanto, de natureza foliar (Figura 330). Estas brácteas classificam-se como férteis ou estéreis consoante suportem, ou não, primórdios seminais. Por sua vez, as brácteas podem tornar-se lenhosas (e.g., Cupressus e Chamaecyparis) ou carnudas (e.g., Juniperus), sendo esta última modificação uma clara adaptação à dispersão das sementes por animais (zoocoria).
Nas Araucariaceae, uma família basal de cupressófitos com grande importância florestal no hemisfério Sul, os estróbilos ♀ exibem apenas brácteas férteis, na superfície das quais se inserem os primórdios seminais (Conway, 2013). Nas antigas taxodiáceas, os primórdios estão localizados na axila ou na base das brácteas: as brácteas são também férteis (Tomlinson & Takaso, 2002). Nas cupressáceas mais evoluídas (e.g., Cupressus), os primórdios seminais inserem-se em várias camadas diretamente no eixo central dos estróbilos: as brácteas são meramente estéreis e protetoras (Figura 329-B). Conclui-se, então, que os estróbilos ♀ são morfologicamente compostos (ramificados) nas antigas taxodiáceas, e secundariamente simples nas Cupressaceae s.str.
Os estróbilos ♀ das pináceas e das cupressáceas mostram, portanto, uma ontogenia e uma morfologia fundamentalmente distintas (Figura 328) e, muito provavelmente, nem sequer partilham uma ancestralidade comum direta. Alguns autores estendem abusivamente o conceito de megasporofilo às brácteas férteis das cupressáceas e de outras famílias de cupressófitos, enquanto outros consideram que não há quaisquer evidências destas estruturas foliares nos estróbilos das gimnospérmicas atuais. O debate evolutivo continua em aberto. Para evitar inconsistências, neste manual e no âmbito das gimnospérmicas, apenas se aplica o termo megasporofilo aos cicadófitos.
A tendência evolutiva para a simplificação do estróbilo ♀ ocorreu de forma convergente e independente em várias linhagens de 'coníferas'. O estróbilo dos zimbros (Juniperus) possui apenas de 1 a poucos primórdios. As Podocarpaceae, uma família com alguma expressão na África tropical e Australásia, retêm apenas um órgão de suporte de primórdios seminais (homólogo da escama ovulífera das pináceas) denominado epimácio, por baixo do qual se insere um número variável de brácteas estéreis, algumas das quais se tornam carnudas e coloridas na maturação (Conway, 2013; Figura 332). As Taxaceae, uma família muito avançada de cupressófitos, representam o caso mais extremo de simplificação do estróbilo ♀: nos teixos (Taxus), diferenciam-se apenas primórdios seminais solitários, encapsulados basalmente por um arilo carnudo na extremidade de ramos curtos. Embora morfologicamente estas estruturas de Ginkgo e Taxus não se assemelhem a estróbilos, os estudos filogenéticos mostram que os ancestrais de ambas as famílias possuíam estróbilos complexos. Por essa razão , a taxonomia moderna considera que todas as estruturas reprodutivas das gimnospérmicas, quer ♀ quer ♂, são, na sua essência evolutiva, estróbilos.
O grupo mais derivado das acrogimnospérmicas, os gnetófitos, reparte-se por três famílias de plantas dióicas (com raras exceções) de morfologia extremamente díspar. Os gnetófitos possuem estróbilos compostos unissexuais, cuja complexidade morfológica não será aqui discutida ao pormenor (Figura 331). Pontualmente, algumas espécies do género Gnetum (Gnetaceae) produzem estróbilos bissexuais (embora funcionalmente ♂) constituídos por anéis com vários verticilos de microsporofilos, distalmente rematados por verticilos de primórdios seminais estéreis. Nestes casos, a gota de polinização segregada pelos primórdios estéreis evoluiu para uma recompensa açucarada destinada a atrair insetos polinizadores (Figura 331-B; Endress, 1996). A tendência para aproximar fisicamente os esporângios ♀ e ♂, embora sem a criação de verdadeiros estróbilos bissexuais funcionais, repete-se na Welwitschia (Endress, 1996). Os estróbilos ♀ destas plantas, porém, têm sempre e apenas verticilos de primórdios seminais. Nos gnetófitos, tanto as estruturas de suporte dos sacos polínicos como os próprios primórdios seminais têm na sua base brácteas fundidas que formam uma estrutura análoga a um perianto floral (Kubitzki, 1990).
As múltiplas convergências evolutivas morfológicas e ecológicas dos gnetófitos com as angiospérmicas (recorde-se que as flores são um estróbilo bissexual) foram, durante quase um século, uma fonte inesgotável de equívocos filogenéticos.Entretanto, a filogenómica moderna veio demonstrar cabalmente que os gnetófitos, ao contrário do que se supunha, não são os parentes evolutivos mais próximos das angiospérmicas (Ran et al., 2018).
Figura 325. Estruturas reprodutivas de Cycadidae. A) Cycas revoluta (Cycadaceae), estróbilo ♀ imaturo. B) Mesma espécie, megasporofilo com primórdios seminais na base. C e D) Encephalartos munchii (Zamiaceae), estróbilos ♀ e ♂, respetivamente. [A e B) fotografias do autor; C e D) Moçambique, cortesia de Pedro Capela].
Figura 326. Estruturas reprodutivas ♀ de Ginkgo biloba (Ginkgoaceae, Ginkgoidae). N.b.: ramos férteis ♀ com dois primórdios seminais, inseridos na base de folhas em forma de leque. [Fotografia do autor].
Figura 327. Estruturas reprodutivas de Pinaceae (Pinidae). A) Estróbilos ♂ de Pinus pinaster aglomerados em grande número ao longo de um ramo do ano. B) Estróbilo ♀ da mesma espécie pouco depois da polinização, com os primórdios seminais isolados do exterior em consequência do crescimento intercalar das escamas ovulíferas. C) Estróbilos ♂ de Cedrus atlantica; n.b.: separação das escamas polínicas e deiscência do pólen de cima para baixo. D) Na mesma espécie, estróbilos ♀; n.b.: grãos de pólen aderidos às escamas ovulíferas. [Fotografias do autor].
Figura 328. Representação diagramática do estróbilo ♀ composto e secundariamente simples nas coníferas (em corte longitudinal). A) Estróbilo ♀ composto de Pinaceae. B) Estróbilo ♀ secundariamente simples de Cupressaceae s. str.. Estruturas caulinares a castanho; estruturas foliares a negro; primórdios seminais a cinzento. [Original].
Figura 329. Estruturas reprodutivas de Cupressaceae (Cupressidae). A) Estróbilos ♂ de Chamaecyparis lawsoniana com sacos polínicos por abrir inseridos na face dorsal de microsporofilos. B) Estróbilo ♀ da mesma espécie; n.b.: primórdios seminais livres em várias camadas na axila das brácteas, com uma gota de polinização exsudada pelo micrópilo; as brácteas depois de maduras dão origem às escamas dos gálbulos (Figura 335-D). C) Estróbilos ♂ de Juniperus oxycedrus; n.b.: posição axilar dos estróbilos, enquanto em Chamaecyparis são terminais. D) Estróbilos ♀ da mesma espécie; n.b.: bractéolas a revestir o caule que suporta o estróbilo; as brácteas são carnudas na maturação (Figura 335-E). [Fotografias do autor].
Polinização e fecundação
O ciclo de vida das plantas do género Pinus é, muitas vezes e de forma muito redutora, assumido como a referência estrutural e evolutiva para todas as gimnospérmicas (Figura 333). É importante ter presente que, embora formem um grupo monofilético, as gimnospérmicas atuais constituem um conjunto de plantas com semente extremamente heterogéneo e antigo (muito anterior à emergência das plantas com flor), com clados que divergiram entre si há centenas de milhões de anos. Nos parágrafos que se seguem, resumo algumas das diferenças no ciclo de vida que separam os cinco grandes grupos de gimnospérmicas atuais: Cycadidae, Ginkgoidae, Cupressidae, Pinidae e Gnetidae. Mas antes de prosseguir, recomenda-se uma leitura atenta do ciclo genérico da Figura 333.
Figura 333. Ciclo de vida das Gimnospérmicas (Pinus pinaster, Pinaceae, Pinidae). Nomenclatura das células do gametófito ♂ de acordo com Fernando et al. (2009). Legenda: R! – meiose. [Tradução e adaptação autorizada de um original de Tomás Díaz González, Univ. Oviedo, Espanha].
Os grãos de pólen (n) diferenciam-se por meiose, e em enorme número, a partir de microsporócitos (2n) no interior de sacos polínicos. Nas angiospérmicas, o micrósporo sofre uma primeira mitose (seguida frequentemente de uma segunda mitose restrita à célula generativa), pelo que o pólen é libertado com 2 ou 3 células e, no momento da fecundação, o gametófito ♂ tem invariavelmente 3 células. As contas são mais complexas nas gimnospérmicas, porque o seu gametófito ♂ (pelo menos no momento da fecundação) é bastante menos reduzido do que o das angiospérmicas. O pólen é libertado com 1 a 5 células, com a notável exceção das podocarpáceas, cujo pólen pode ultrapassar as 40 células no momento da dispersão. O grão de pólen das Taxaceae, por outro lado, é libertado contendo apenas uma célula; para todos os efeitos, é um micrósporo puro, um caso único entre as plantas com semente (Anderson & Owens, 2000).
No momento da libertação dos gâmetas (i.e., já às portas dos arquegónios), o microgametófito maduro tem, por exemplo, 3 células nas Cupressaceae, 4 nas Taxaceae, 5 nas Cycadidae, 6 no Ginkgo e nas Pinaceae, e dezenas nas Podocarpaceae (Fernando et al., 2009). Ao invés do que sucede nas angiospérmicas, os especialistas conseguem ainda reconhecer no microgametófito das gimnospérmicas (exceto nas cupressáceas) resíduos evolutivos do protalo (1 ou 2 células protaliais estéreis) e do anterídio (1 célula anteridial). Contudo, à semelhança das angiospérmicas, ocorre sempre a diferenciação de uma célula do tubo e de uma célula generativa (que dará origem, após a polinização, a 2 gâmetas ♂, com raras exceções) (Fernando et al., 2009).
Ao contrário do que se verifica nas angiospérmicas, na esmagadora maioria das gimnospérmicas a diferenciação funcional dos megasporócitos (2n) depende do estímulo químico da polinização: é, portanto, posterior a esta. O megasporócito gera, por meiose, 4 megásporos (n), um dos quais (geralmente, o calazal, i.e., o mais afastado do micrópilo) sobrevive, germina e dá origem ao gametófito ♀. O gametófito ♀ maduro das gimnospérmicas contém milhares de células e diferencia múltiplos arquegónios: 2 a 5 nas 'coníferas', geralmente em muito maior número nas Ginkgoidae e Cycadidae, e 1 a 3 em Ephedra (o mais basal dos três géneros de Gnetidae) (Fernando et al., 2009). Curiosamente, as células do gametófito ♀ das Ginkgoidae são clorofiladas (verdes). Cada arquegónio tem à sua custódia uma única oosfera. O desenvolvimento de arquegónios típicos, contudo, não é claro em dois géneros muito derivados de Gnetidae — Welwitschia (Figura 7) e Gnetum —, tal como, aliás, acontece nas angiospérmicas (Carmichael & Friedman, 1995).
Os grãos de pólen são transportados massivamente pelo vento (polinização anemófila), sendo diretamente capturados pelos primórdios seminais, os quais, para o efeito, secretam para o exterior do micrópilo uma gota de polinização (Figura 327-A, B, C), frequentemente visível a olho nu. Nas 'coníferas', a conjugação aerodinâmica da forma dos ramos, folhas e estróbilos gera pequenos vórtices de ar que conduzem os grãos de pólen diretamente em direção ao micrópilo dos primórdios seminais (Niklas, 1984). As Cycadidae e as Gnetidae são, contudo, secundariamente polinizadas por insetos (entomofilia). Em algumas espécies destes dois grupos, a própria gota de polinização funciona como recompensa alimentar açucarada.
Os açúcares dissolvidos na gota de polinização reduzem as perdas de água por evaporação e, ao aumentarem drasticamente a viscosidade do líquido, diminuem a probabilidade da gota se soltar do micrópilo pela ação direta do vento e da agitação mecânica dos ramos (Lunau, 2002). Ainda assim, a folhagem de géneros como Chamaecyparis e Cupressus fica frequentemente pegajosa devido à acumulação de gotas que se destacam dos primórdios seminais no pico do período de polinização. Os grãos de pólen afundam-se na gota de polinização (ou são arrastados ativamente quando esta é fisiologicamente reabsorvida pela planta) e entram no primórdio. Em seguida, a porção da gota que fica exposta ao exterior seca e sela hermeticamente o micrópilo. O microgametófito fica assim protegido no interior da câmara polínica (Chamberlain, 1935), num ambiente mantido mais ou menos assético pela ação de proteínas antimicrobianas previamente dissolvidas na gota de polinização (Poulis et al., 2005).
No interior da câmara polínica, o pólen germina na superfície do nucelo, rompe a esporoderme (exina) e diferencia um tubo polínico. O tubo penetra o nucelo de forma intercelular (digerindo a lamela média), ao mesmo tempo que o microgametófito vive uma sequência final de mitoses que desemboca na formação dos gâmetas ♂. O tubo polínico tem de vencer uma barreira mecânica de 0,1 a 3 mm de espessura de nucelo, um tecido que já não diferencia uma barreira nas angiospérmicas (Williams, 2008). O tubo polínico das gimnospérmicas mantém uma continuidade citoplásmica total entre a sua extremidade de crescimento e o grão de pólen original; por essa razão, é muito mais curto do que o tubo das angiospérmicas (Fernando et al., 2009). Em contraste, no tubo polínico das angiospérmicas diferenciam-se, a cada passo do seu avanço, tampões isolantes de calose que mantêm as células espermáticas e o citoplasma ativo sequestrados apenas na extremidade distal do tubo, permitindo que este atinja comprimentos assinaláveis (e.g., descendo ao longo de todo o estilete do milho) (Lord, 2000).
Nas Ginkgoidae e nas Cycadidae, o tubo polínico (que tem uma função meramente haustorial/alimentar) rompe-se na proximidade da câmara arquegonial: cada tubo liberta dois gâmetas flagelados (anterozoides) que nadam ativamente no fluido rumo às oosferas (zooidogamia ou sifonogamia imperfeita). A observação de gâmetas ♂ flagelados nestas plantas de semente estabeleceu uma conexão evolutiva entre os 'pteridófitos' e as gimnospérmicas, sendo considerada uma das mais importantes descobertas científicas botânicas do século XIX. Nas Cupressidae, Pinidae e Gnetidae — i.e., no grosso das gimnospérmicas atuais —, o tubo polínico conduz e coloca as células espermáticas imóveis em contacto direto com as oosferas (sifonogamia verdadeira).
No Ginkgo biloba, o intervalo que medeia entre a polinização e a fecundação é de 4 a 5 meses, caindo em seguida os primórdios recém-fecundados ao solo (Treici, 2007). Este intervalo ronda os 6 a 12 meses nas Cycadidae, e pode estender-se de 3 meses a uns impressionantes 24 meses nalgumas 'coníferas' (Singh, 1978 cit. em Williams, 2009). Nas Gnetidae, a dinâmica é muito mais rápida: decorre apenas 1 semana em Gnetum e 10 a 36 horas em Ephedra (Fernando et al., 2009). Cada oosfera é fecundada por um único núcleo espermático. Em dois géneros de Gnetidae (Gnetum e Ephedra) foi descoberto um esboço evolutivo de dupla fecundação; contudo, o tecido nutritivo de reserva permanece invariavelmente haploide, tal como nos restantes grupos de gimnospérmicas, não se formando um endosperma verdadeiro (Carmichael & Friedman, 1995; Friedman, 2014).
A existência comum de múltiplos arquegónios num único megagametófito gera frequentemente mais do que um embrião viável (poliembrionia simples; simple polyembryony) e, implicitamente, vários embriões em cada primórdio seminal. Este fenómeno é quase universal nas gimnospérmicas. Sobretudo em alguns géneros de Pinaceae, ocorre também, e com grande frequência, um outro tipo de embrionia, a poliembrionia por clivagem (cleavage polyembryony), que se verifica quando um único embrião jovem se cinde vegetativamente em vários outros embriões idênticos. Em Pinus, é comum o início da formação de até 8 embriões. Em ambos os sistemas, porém, a competição interna dita que geralmente apenas um embrião sobrevive até à fase final — as sementes maduras de gimnospérmicas raramente contêm mais do que um embrião viável.
Não se conhecem nas gimnospérmicas sistemas genéticos de autoincompatibilidade pré-zigótica (antes da fecundação) nem mecanismos de seleção de gâmetas (competição de tubos polínicos) similares aos que ocorrem no estilete das angiospérmicas (vd. «Sistemas de autoincompatibilidade» e «Competição do pólen. Seleção de gâmetas»). Foi proposto que a poliembrionia simples e por clivagem funciona, nestas plantas, como um mecanismo alternativo de seleção (pós-zigótico) da melhor descendência (Zavada & Taylor, 1986). Este sistema de triagem competitiva atua internamente enquanto os embriões são ainda muito pequenos, mas, ainda assim, é substancialmente menos eficiente do que os sistemas pré-zigóticos das angiospérmicas e acarreta custos energéticos incomparavelmente superiores para a planta materna.
As reservas nutritivas das sementes das gimnospérmicas resumem-se a um endosperma primário haploide, formado antes da fecundação, constituído exclusivamente por tecido gametofítico de origem materna (as próprias células haploides do saco embrionário). Este endosperma primário é um gametófito ♀ muito modificado e intumescido, constituindo uma estrutura de reserva sem qualquer paralelo nas angiospérmicas.
Nas Ginkgoidae e nas Cycadidae, o primórdio seminal atinge a sua dimensão final de semente logo depois da polinização, mas ainda antes da fecundação ocorrer. Este padrão de crescimento constitui um investimento reprodutivo de elevadíssimo risco energético, porque se o primórdio não for fecundado e abortar, a planta deita a perder todo o investimento em biomassa e reservas. As 'coníferas' (Cupressidae + Pinidae) são evolutivamente mais eficientes porque o crescimento massivo dos primórdios e a acumulação de reservas só ocorrem após a fecundação, sendo a planta capaz de realocar atempadamente parte da energia dos primórdios não fecundados. As angiospérmicas, contudo, otimizaram este processo ao extremo da eficiência, uma vez que só começam a acumular reservas no endosperma (através da dupla fecundação) se a singamia for efetivamente bem-sucedida.
O intervalo total entre a polinização da flor/cone e a maturação final das sementes ronda 1 ano na grande maioria das gimnospérmicas. É um pouco mais curto no Ginkgo biloba (Treici, 2007). Em algumas espécies de Cycas (Cycadidae), o processo estende-se por impressionantes 2,5 anos (Pant, 2002). As sementes dos pinheiros (Pinus) amadurecem tipicamente em 2 anos (e.g., pinheiro-bravo, Pinus pinaster) ou até 3 anos (e.g., pinheiro-manso, Pinus pinea). É igualmente frequente as sementes caírem ao solo de forma ainda imatura (e.g., Ginkgo, cicas e Gnetum), terminando o desenvolvimento embrionário já na folhada. Como vimos no capítulo anterior, as angiospérmicas reproduzem-se, por oposição, com uma enorme rapidez. No Ginkgo e nas Cycadidae, ao contrário das 'coníferas', as sementes maduras não suportam a desidratação — são sementes recalcitrantes. As sementes das gimnospérmicas apresentam geralmente dois cotilédones embrionários (embora sejam numerosos verticilados no género Pinus; Figura 334) e são extremamente ricas em lípidos e proteínas.
Frutificações e sementes
As sementes do ginkgo (Ginkgo biloba, Ginkgoaceae) e dos teixos (Taxus, Taxaceae) diferenciam-se e amadurecem sem qualquer proteção estrobilar lenhosa. As sementes de ginkgo desenvolvem uma sarcotesta carnuda e espessa, com um odor desagradável a ácido butírico na maturação (assemelhando-se a manteiga rançosa) — razão pela qual o planeamento urbano evita a plantação de árvores ♀ em passeios e jardins. Os ancestrais dos ginkgos foram certamente dispersos endozoocoricamente por dinossauros herbívoros no Mesozoico e pela megafauna mamífera no Plistocénico (Del Tredici, 1989). Hoje em dia, o Ginkgo biloba (a única espécie atual sobrevivente de toda a sua subclasse) é um fóssil vivo que depende do Homem para se propagar e dispersar (antropocoria). Nos teixos (Taxus, Taxaceae), as sementes nuas surgem basalmente envolvidas por uma estrutura carnuda e vermelha (arilo), muito doce e comestível para as aves (embora a semente em si, e toda a folhagem da árvore, sejam mortalmente tóxicas para a maioria dos mamíferos). O arilo atua assim como a recompensa perfeita para a dispersão endozoocórica (Figura 335-A). Anatomicamente, esta estrutura tem origem foliar (resulta da fusão de duas folhas modificadas), não cabendo, num sentido botânico estrito, no conceito clássico de arilo (Dörken et al., 2019).
Designa-se por frutificação (Figura 335) o estróbilo ♀ maduro, mono ou plurispérmico, das gimnospérmicas. O fruto, num sentido botânico estrito, resulta exclusivamente do desenvolvimento das paredes de um ovário após a fecundação (tem origem carpelar): o fruto é, portanto, uma sinapomorfia (característica exclusiva) das angiospérmicas. As frutificações lenhosas das gimnospérmicas são, assim, estruturas análogas (e não homólogas) aos frutos secos das plantas com flor.
Nas 'coníferas' reconhecem-se dois tipos fundamentais de frutificações:
- Gálbulos (ougálbulas): estróbilos de forma tendencialmente globosa, compostos por brácteas normalmente peltadas (em forma de guarda-chuva ou escudo) que se inserem mais ou menos no mesmo ponto do eixo central; e.g., frutificações lenhosas dos ciprestes (Cupressus, Cupressaceae). Apresentam um subtipo ecológico particular: os gálbulos baciformes — gálbulos de brácteas intimamente fundidas e carnudas, morfologicamente muito semelhantes a uma baga ou drupa (funcionando como tal para atrair aves), característicos dos zimbros (Juniperus, Cupressaceae) e de membros das Podocarpaceae;
- Pinhas: estróbilos alongados ou cónicos, compostos por escamas ovulíferas lenhosas imbricadas (e.g., pinhas de pinheiro [Pinus, Pinaceae]) ou brácteas espessas (e.g., cones das araucárias [Araucaria, Araucariaceae]) que se inserem ao longo de um eixo central desenvolvido.
A dispersão das 'coníferas' faz-se, sobretudo, sob a forma de semente libertada a partir de estróbilos deiscentes. Nos abetos (Abies) e nos cedros (Cedrus), os estróbilos lenhosos maduros desintegram-se completamente na própria árvore, libertando-se em simultâneo do eixo central (e caindo ao solo) as escamas ovulíferas e as sementes. Nas restantes espécies de pináceas, as escamas ou brácteas do estróbilo abrem higroscopicamente na maturação (afastando-se do eixo) para que a semente possa ser arrastada e dispersa pela força do vento (anemocoria). Algumas frutificações de gimnospérmicas (particularmente no género Pinus) são marcadamente serotinas, i.e., mantêm-se seladas com resina durante anos e apenas abrem as escamas para dispersar as sementes em resposta a um estímulo térmico extremo, concretamente pela ação da passagem do fogo de um incêndio florestal (como acontece com os cones fechados do pinheiro-bravo) (Tapias et al.,2001).
Para auxiliar a sua aerodinâmica, géneros como Araucaria, Agathis, Pinus, Cedrus, Tsuga, Abies, Picea e tantos outros clados de coníferas, desenvolvem sementes aladas, cuja asa membranosa não é mais do que o resultado da expansão lateral das camadas superficiais do tegumento durante a maturação. Uma notável adaptação à anemocoria por semente alada ocorre também na Welwitschia mirabilis [Gnetidae], que usa o vento do deserto da Namíbia para dispersar as suas sementes.
Por outro lado, nas 'coníferas' que desenvolveram frutificações de textura carnuda, não se dispersa a semente nua; dispersa-se a frutificação inteira através da ingestão e transporte por animais frugívoros (zoocoria). Exemplos clássicos são os já referidos zimbros (Juniperus, Cupressaceae), os Cephalotaxus (Taxaceae) e as espécies de Podocarpaceae. Estruturas carnudas de origem foliar (brácteas modificadas) de ajuda à dispersão zoocórica ocorrem também nos gnetófitos dos géneros Ephedra e Gnetum. Da mesma forma ecológica, as sementes primitivas dos cicadófitos, por estarem providas de uma espessa e nutritiva sarcotesta, são ativamente procuradas e dispersas por mamíferos terrestres ou morcegos frugívoros, havendo também espécies insulares cujas sementes esponjosas flutuam eficazmente na água do mar (hidrocoria) (Dehgan & Yuen, 1983).
Figura 330. Natureza foliar das brácteas do estróbilo ♀ das Cupressaceae: gálbulos teratogénicos de Cryptomeria japonica (Cupressaceae, Cupressidae). O meristema que deu origem a este gálbulo reverteu a uma condição vegetativa depois de diferenciar as brácteas do estróbilo ♀. Provavelmente, manteve-se funcional até que a morte programada das células do estróbilo maduro interrompesse as suas conexões vasculares com o ramo onde se insere. [Ilha de S. Miguel, Açores; fotografia do autor].
Figura 331. Estruturas reprodutivas dos gnetófitos. A) Gnetum africanum (Gnetaceae): 1 e 4 – hábito; 2 – pormenor do estróbilo ♂; 3 – microsporofilo com várias brácteas na base; 5 – estróbilo ♀; 6 – semente. B) Gnetum gnemon: estróbilo ♂ com verticilos de microsporofilos encimados por verticilos de primórdios seminais estéreis que, apesar de tudo, produzem uma gota de polinização (visível na figura). C) Ephedra fragilis subsp. fragilis (Ephedraceae): pormenor de estróbilo ♀ com primórdios seminais revestidos com brácteas; a hipótese de que as peças bracteolares de uma gnetácea estão na origem do perianto floral é tentadora, mas falsa (volume II). D) Na mesma espécie, estróbilos maduros constituídos, neste caso, por uma semente madura rodeada por brácteas carnudas e vermelhas; n.b.: caules articulados. [A)http://www.prota.org; B) cortesia de Kevin C. Nixon e http://www.plantsystematics.org; C e D) cortesia de Miguel Porto e de Flora-on].
Figura 332. Cone ♀ de Podocarpaceae (Pinidae). Cone maduro de Podocarpus angustifolius, uma árvore endémica de Cuba. O cone das podocarpáceas tem geralmente apenas um primórdio; cada primórdio está envolvido por uma escama ovulífera carnuda, o epimácio. Algumas brácteas situadas na base do cone são carnudas na maturação, muitas vezes vermelhas, para atraírem dispersores. [Fotografia do autor].
Figura 333. Ciclo de vida das Gimnospérmicas (Pinus pinaster, Pinaceae, Pinidae). Nomenclatura das células do gametófito ♂ de acordo com Fernando et al. (2009). Legenda: R! – meiose. [Tradução e adaptação autorizada de um original de Tomás Díaz González, Univ. Oviedo, Espanha].
Figura 334. Cotilédones nas gimnospérmicas. Plântula de pinheiro-bravo com 11 cotilédones. [Cortesia de Nuno Gomes].
Figura 335. Frutificações das 'coníferas'. A) Semente solitária de teixo (Taxus baccata, Taxaceae) envolvida por um arilo vermelho; n.b.: bractéolas a revestir o caule que suporta a semente. B) Estrutura de uma pinha de pinheiro-manso (Pinus pinea, Pinaceae). C) Pinha de pseudotsuga (Pseudotsuga menziesii, Pinaceae); n.b.: brácteas tetrizes exsertas na axila das quais se inserem escamas ovulíferas arredondadas, cada uma com duas sementes apensas (não visíveis na fotografia). D)Gálbulos de cipreste-do-óregon (Chamaecyparis lawsoniana, Cupressaceae); n.b.: sementes aladas na axila de brácteas peltadas (em forma de guarda-chuva). E) Gálbulos baciformes de sabina-das-praias (Juniperus turbinata, Cupressaceae). [Fotografias do autor].


 B)
B)
 D)
D)

 B)
B)
 D)
D)